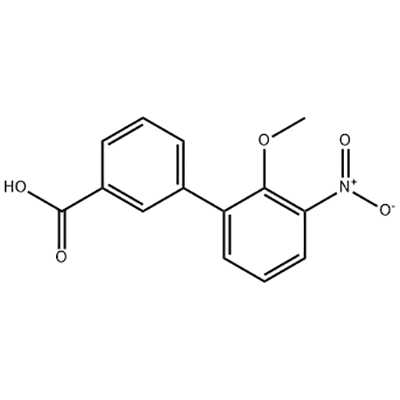
2′-Methoxy-3′-nitro-biphenyl-3-carboxylic ອາຊິດ
2′-Methoxy-3′-nitro-biphenyl-3-carboxylic ອາຊິດ
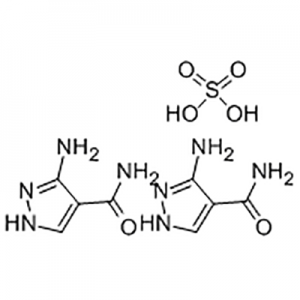
2'-Methoxy-3'-nitro-biphenyl-3-carboxylic acid ຖືກນໍາໃຊ້ເປັນຕົວກາງຂອງ Eltrombopag .
Eltrombopag, ພັດທະນາໂດຍ GlaxoSmithKline (GSK) ໃນປະເທດອັງກິດແລະຕໍ່ມາໄດ້ຮ່ວມກັນພັດທະນາກັບ Novartis ໃນສະວິດເຊີແລນ, ເປັນໂມເລກຸນຂະຫນາດນ້ອຍທີ່ບໍ່ໄດ້ຮັບການອະນຸມັດຄັ້ງທໍາອິດແລະພຽງແຕ່ peptide TPO receptor agonist ໃນໂລກ.Eltrombopag ໄດ້ຮັບການອະນຸມັດໂດຍ US FDA ໃນປີ 2008 ສໍາລັບການປິ່ນປົວ idiopathic thrombocytopenic purpura (ITP), ແລະໃນປີ 2014 ສໍາລັບການປິ່ນປົວພະຍາດເລືອດຈາງ aplastic ຮ້າຍແຮງ (AA).ມັນຍັງເປັນຢາທໍາອິດທີ່ໄດ້ຮັບການອະນຸມັດໂດຍ FDA ສະຫະລັດສໍາລັບການປິ່ນປົວ AA ໃນ 30 ປີທີ່ຜ່ານມາ.
ໃນເດືອນທັນວາ 2012, FDA ສະຫະລັດໄດ້ອະນຸມັດ Eltrombopag ສໍາລັບການປິ່ນປົວ thrombocytopenia ໃນຄົນເຈັບທີ່ມີໂຣກຕັບອັກເສບ C ຊໍາເຮື້ອ (CHC), ດັ່ງນັ້ນຄົນເຈັບຕັບອັກເສບ C ທີ່ມີການຄາດຄະເນທີ່ບໍ່ດີເນື່ອງຈາກຈໍານວນ platelet ຕ່ໍາສາມາດເລີ່ມຕົ້ນແລະຮັກສາການປິ່ນປົວດ້ວຍມາດຕະຖານ interferon ສໍາລັບພະຍາດຕັບ.ໃນວັນທີ 3 ກຸມພາ, 2014, GlaxoSmithKline ປະກາດວ່າ FDA ໄດ້ອະນຸມັດຄຸນສົມບັດຂອງຢາປິ່ນປົວແບບກ້າວກະໂດດຂອງ Eltrombopag ສໍາລັບການປິ່ນປົວພະຍາດ hemopenia ໃນຄົນເຈັບທີ່ເປັນພະຍາດເລືອດຈາງທາງເຄມີທີ່ຮຸນແຮງ (SAA) ທີ່ບໍ່ຕອບສະຫນອງຢ່າງເຕັມສ່ວນກັບ immunotherapy.ໃນເດືອນສິງຫາ 24, 2015, FDA ສະຫະລັດໄດ້ອະນຸມັດ Eltrombopag ສໍາລັບການປິ່ນປົວ thrombocytopenia ໃນຜູ້ໃຫຍ່ແລະເດັກນ້ອຍທີ່ມີອາຍຸ 1 ປີຂຶ້ນໄປທີ່ມີພູມຕ້ານທານ thrombocytopenia ຊໍາເຮື້ອ (ITP) ທີ່ມີການຕອບສະຫນອງບໍ່ພຽງພໍກັບ corticosteroids, immunoglobulins ຫຼື splenectomy.ໃນວັນທີ 4 ມັງກອນ 2018, Eltrombopag ໄດ້ຖືກອະນຸມັດໃຫ້ຢູ່ໃນປະເທດຈີນສໍາລັບການປິ່ນປົວໂຣກ thrombocytopenia ພູມຕ້ານທານຂັ້ນຕົ້ນ (ITP).



![pentamethylene bis[1-(3,4-dimethoxybenzyl)-3,4-dihydro-6,7-dimethoxy-1H-isoquinoline-2-propionate], dixalate](http://cdn.globalso.com/jindunchem-med/image281-300x300.png)

![Casp ungin Acetate;Caspofungin acetate;Cancidas;Caspofungin acetate [USAN:BAN:JAN];](http://cdn.globalso.com/jindunchem-med/fbe17385-300x300.jpg)